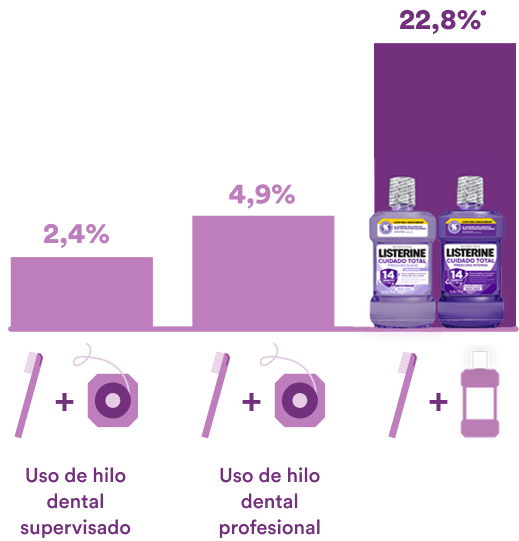
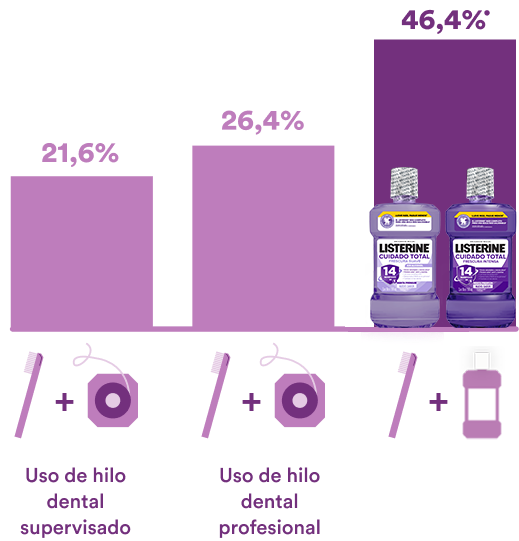
¿Qué causa la disbiosis en la caries dental?
La cavidad bucal tiene la segunda microbiota más grande y diversa después del intestino, alberga más de 700 especies de bacterias y tiene dos tipos de superficies en las que las bacterias pueden colonizar: los tejidos duros y blandos de los dientes, y la mucosa bucal.
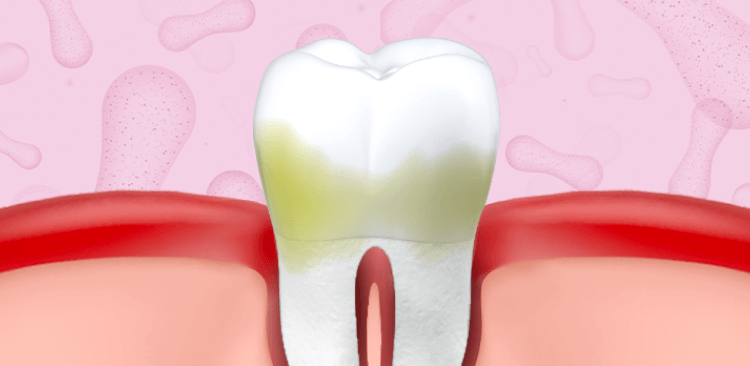
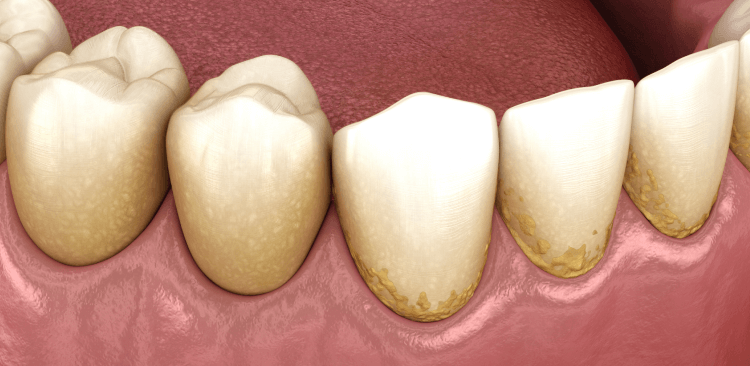
Estas superficies proporcionan un entorno rico en el que pueden prosperar los microorganismos formando la biopelícula, la cual se denomina placa dental cuando se desarrollan en los dientes.1, 2
Se creía que estas bacterias eran agentes infecciosos y que los bebés adquirían este patógeno de sus madres solo después de la erupción de los dientes primarios4. En consecuencia, los tratamientos clínicos se enfocaron en prevenir o retrasar la transmisión de estos organismos, junto con intentos de suprimir o incluso eliminar el streptococo mutans en la cavidad bucal, con sustancias antibacterianas tópicas y vacunas. Sin embargo, este paradigma "un patógeno, una enfermedad" ahora ha sido reemplazado por un concepto holístico de una comunidad microbiana como la entidad de patogenicidad.5
Diversos estudios en personas de diferentes edades y con diferentes dietas en el mundo, han demostrado diferencias sustanciales en la composición de las biopelículas que recubren las lesiones de caries.
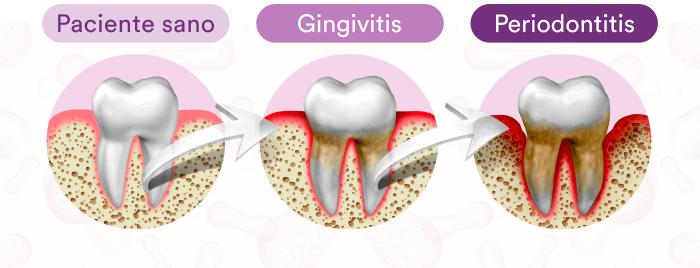
Por lo tanto, el desarrollo de una lesión de caries se asocia con un cambio disbiotico en el equilibrio de la microbiota dental residente. El principal impulsor de tal cambio es el consumo frecuente de azúcares en la dieta.
La introducción temprana de sacarosa en la vida de un bebé promueve el establecimiento de una microbiota cariogénica y la colonización sucesiva de nuevas superficies dentales. Además, aumenta la preferencia de los niños por los dulces, lo que resulta en un mayor consumo de azúcar en alimentos y bebidas.7
Por otra parte la frecuencia del consumo de azúcares libres (añadidos por el productor o por el consumidor) e hidratos de carbono, especialmente en niños y adultos genera una respuesta dosis-dependiente; con una mayor ingesta aumenta el riesgo de caries por la producción repetida de ácidos y el mantenimiento de un pH muy bajo en la biopelícula dental; impidiendo la reposición fisiológica de minerales en el ciclo de desmineralización/remineralización.8
El objetivo de la prevención primaria es por consiguiente preservar y mantener la simbiosis en la biopelícula bucal mientras que el objetivo de la prevención secundaria es restaurar un microbioma no saludable mediante la eliminación de estos impulsores de cambios adversos.

Según las recomendaciones de la OMS
Vale la pena recalcar que la caries dental es una enfermedad no transmisible de etiología multifactorial que comparte factores de riesgo con otras enfermedades no transmisibles de alta prevalencia, como la obesidad, la diabetes y las enfermedades cardiovasculares; la ingesta de azúcar es uno de estos factores de riesgo.10

Teniendo en cuenta la evidencia científica disponible la evaluación individual del riesgo de caries (CRA) se considera de las mejores prácticas en la toma de decisiones de manejo de caries.11, 12
Actualmente existe un acuerdo para la evaluación de riesgos, con preferencia de un modelo multifactorial sobre una evaluación de factor único, ya que considera factores de protección, factores de riesgo sociales/médicos/conductuales y factores clínicos, poniendo la salud bucal dentro de la salud general.13
CCI considera factores protectores el uso de ≥ 1000 ppm de pasta dental fluorada dos veces al día, cuidado dental preventivo y fluoruro comunitario accesible. Este modelo además clasifica al paciente en dos categorías de riesgo:

Una versión simplificada que permite un manejo práctico del paciente donde se involucra el autocuidado en casa, el enfoque clínico y los intervalos de atención basados en el riesgo.14
Pero tal vez lo más relevante sea la comunicación equipo odontológico-paciente y el involucramiento en el cuidado de su salud bucal. Al tomar conciencia de su riesgo de enfermedad se aumenta la adherencia y la satisfacción de los pacientes con el cuidado dental.
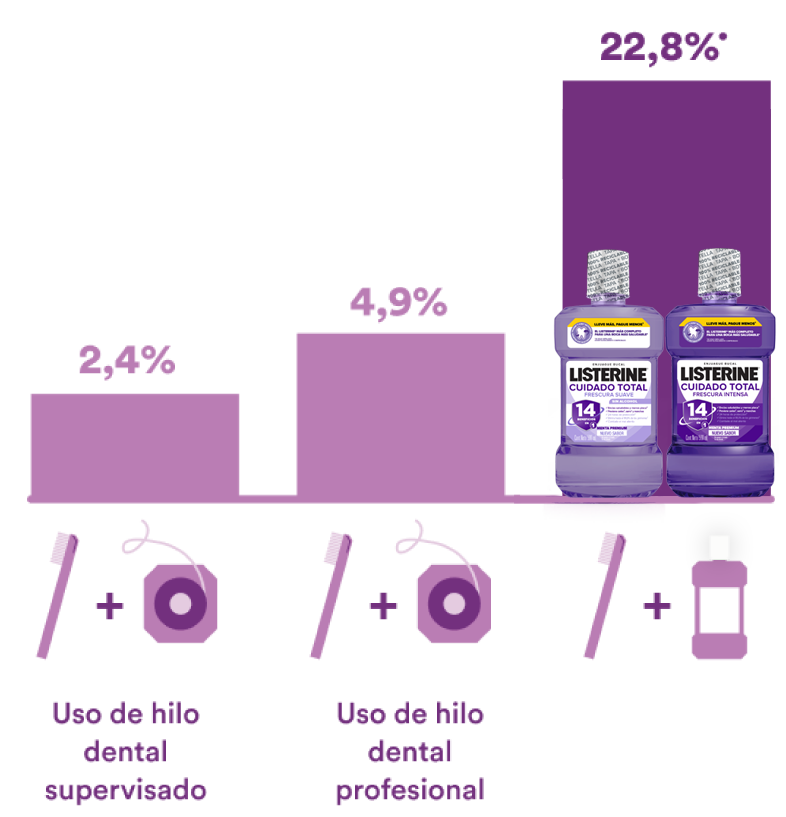
LISTERINE® CUIDADO TOTAL ZERO
Es el enjuague bucal libre de alcohol y con sabor más suave. Su exclusiva fórmula con 4 aceites esenciales, flúor y cloruro de zinc, elimina hasta el 99.9% de las bacterias12, protegiendo y manteniendo las encías saludables.

Esta presentación sin alcohol es apta para niños a partir de los 6 años, edad en la que suelen tener más caries por el consumo de dulce, además de inculcarles una buena rutina de limpieza bucal desde pequeños.

Si este tema le interesó, descubra también nuestras recomendaciones.
- 1. Zaura E, Nicu EA, Krom BP, Keijser BJ. Acquiring and maintaining a normal oral microbiome: Current perspective. Front Cell Infect Microbiol 2014;4:85.
- 2. Dewhirst FE, Chen T, Izard J, Paster BJ, Tanner AC, Yu WH, et al. The human oral microbiome. J Bacteriol 2010;192:5002,Äê17.
- 3. SimoÃÅn-Soro A, Mira A. Solving the aetiology of dental caries. Trends Microbiol 2015; 23: 76-82.
- 4. Schwendicke F, Dorfer C E, Schlattmann P, Foster Page L, Thomson W M, Paris S. Socioeconomic inequality and caries: a systematic review and meta-analysis. J Dent Res 2015; 94: 10-18.
- 5. Colombo A P V, Tanner A C R. The Role of Bacterial Biofilms in Dental Caries and Periodontal and Peri-implant Diseases: A Historical Perspective. J Dent Res 2019; 98: 373-385.
- 6. Chaffee BW, Feldens CA, Rodrigues PH, Vítolo MR. Feeding practices in infancy associated with caries incidence in early childhood. Community Dent Oral Epidemiol. 2015 Aug;43(4):338-48. doi.org/10.1111/cdoe.12158.
- 7. Ventura AK, Worobey J. Early influences on the development of food preferences. Curr Biol. 2013 May;23(9):R401-8. doi.org/10.1016/j.cub.2013.02.037.
- 8. Peres MA, Sheiham A, Liu P, Demarco FF, Silva AE, Assunção MC, et al. Sugar consumption and changes in dental caries from childhood to adolescence. J Dent Res. 2016 Apr;95(4):388-94.
- 9. World Health Organisation. Oral Health: Achieving better oral health as part of the universal health coverage and noncommunicable disease agendas towards 2030. Geneva: World Health Organisation, 2020.
- 10. Fisberg M, Kovalskys I, Gómez G, et al. Total and added sugar intake: assessment in Eight Latin American countries. Nutrients. 2018 Mar;10(4):389.
- 11. Martignon S, Pitts NB, Goffin G, Mazevet M, Douglas GV, Newton JT, et al. CariesCare practice guide: consensus on evidence into practice. Br Dent J. 2019 Sep;227(5):353-62.
- 12. Mejàre I, Axelsson S, Dahlén G, Espelid I, Norlund A, Tranæus S, et al. Caries risk assessment: a systematic review. Acta Odontol Scand. 2014 Feb;72(2):81-91.
- 13. Senneby A, Mejàre I, Sahlin NE, Svensäter G, Rohlin M. Diagnostic accuracy of different caries risk assessment methods: a systematic review. J Dent. 2015 Dec;43(12):1385-93.
- 14. Cagetti MG, Bontà G, Cocco F, Lingstrom P, Strohmenger L, Campus G. Are standardized caries risk assessment models effective in assessing actual caries status and future caries increment? A systematic review. BMC Oral Health. 2018;18(1):123.
- 15. Elimina el 99.9% de las bacterias que causan la placa y el mal aliento. Estudios FCLGBP0028 y FCLGBP0048.